Методика розщеплення альвеолярного гребеня. Особливості вибору тактики. Частина 2
20.08.2020
Статті
Головний лікар медичного центру «ІМПЕРІЯ ДЕНТІС»
Лікар стоматолог-хірург вищої категорії Дегасюк В.В.
Мета: дослідити методику розщеплення гребеня. З’ясувати переваги розщеплення за допомогою ультразвукової апаратури та операційну тактику, в залежності від клінічної ситуації.
Матеріали та методи. У дослідженні приймали участь 26 осіб з шириною альвеолярного гребеня від 2,9 до 5,5 мм. Розпил кортикальної кістки виконували або за допомогою оборотної фрези для кутового наконечника, або за допомогою апарата Piezotome Solo (Satelec, Aсteon). Створений кістковий дефект заповнювали кістковим матеріалом BIO GEN mix (Biotek). Ортопедична конструкція на імплантати виготовлялась відтерміновано.
Результати. Збільшення ширини альвеолярного паростка по верхівці альвеолярного гребеня на 2.5 - 4.0 мм, що складало від 30% до 110%; вертикальна резорбція складала в середньому 1.05 мм (при формуванні повного клаптя та проведенні розпилу фрезами), 0.6 мм (при формуванні повного клаптя та проведенні розпилу за допомогою Piezotome Solo), 0.4 мм (при формуванні неповного клаптя, використанні вільного трансплантата та проведення розпилу Piezotome Solo).
У першій частині статті ми розглядали сучасні особливості роботи з альвеолярним паростком під час кісткової аугментації за методикою розщеплення кісткового гребеня. Друга частина буде присвячена менеджменту м’яких тканин навколо ділянки розщеплення.
Класично, методика розщеплення альвеолярного паростка передбачала формування повного клаптя, проведення розпилу по верхівці альвеолярного гребеня та послаблюючих розпилів кортикальної пластинки вестибулярно. Техніки, які передбачали формування повного клаптя, супроводжувались формуванням блюдцеподібного заглиблення з вестибулярної сторони [7].
З часом, поводження з кісткою та м’якими тканинами стало більш обережне. Відомо, що існують остеогенні клітини з набором потенційних остеоіндуктивних можливостей, які знаходяться в остеогенному шарі окістя (так званий камбіальний шар). Існує думка, що під час відшарування окістя цей шар значно травмується і погано відновлюється [9].
Нині досить багато клініцистів використовують щадне поводження з тканинами. Збереження не відшарованого окістя дозволяє запобігти резорбції кістки. Досі деякі автори завжди формують повний клапоть (Holtzclaw et all, 2010; Blus et all, 2006; Danza et all, 2009), інші пропонують збереження окістя (Vercellotti et all, 2000; Sethi et all, 2000) під час проведення кісткової аугментації за методикою розщеплення. [8]
Також, досить цікавим є питання збільшення об’єму м’яких тканин одномоментно з кістковою аугментацією. Класично вважається, що м’якотканинна аугментація не є доцільною перед кістковою аугментацією або одночасно з нею. Це обґрунтовується тим, що під час проведення операцій зі збільшення об’єму кістки досить часто втрачається глибина присінку порожнини рота, що з часом призводить до втрати кількості прикріплених кератинізованих ясен і міграції рухливої слизової коронально. В нашій практиці ми, все ж таки, застосовуємо комбінацію мякотканинної та кісткової аугментацій. Одними з таких операцій можна вважати деякі випадки розщеплення альвеолярного гребеня. На нашу думку, застосування м’якотканинного трансплантата під час проведення методики розщеплення має такі переваги:
1. Надає можливість збільшення товщини м’яких тканин над ділянкою імплантації.
2. Вважається, що трансплантація м’яких тканин у зону кісткової підсадки може забезпечувати останню мезинхімальними клітинами [10].
3. Покращує умови для адекватного м’якотканинного прикриття.
Звісно, не виключена можливість часткового або повного некрозу трансплантата. Але в нашій практиці, це ніколи не призводило до значного погіршення клінічної ситуації.
Обов’язковими умовами для пересадки м’яких тканин є збереження не ушкодженого та не відшарованого окістя на альвеолярному гребені для можливості забезпечення живлення трансплантату. Важливим є збереження загальних принципів роботи з вільними клаптями:
· Трансплантат повинен бути рівномірним за товщиною. Адже не рівну поверхню дуже важко, майже неможливо, рівномірно притиснути до реципієнтної ділянки та забезпечити живлення.
· Основа трансплантату повинна складатися виключно зі сполучної тканини. Наявність жирової тканини недопустима.
· Надзвичайно важливим є надійна фіксація пересадженого клаптя до приймаючої ділянки. Рухливість трансплантата призведе до того, що судини не зможуть прорости в нього та відбудеться некроз. Ми обов’язково фіксуємо трансплантат по периметру до окістя, а далі накладаємо перехресні шви. Таким чином ми попереджаємо виникнення «мертвого простору» під вільним клаптем.
Клінічний випадок
Пацієнтка К. звернулась у клініку з метою протезування ділянки адентії на нижній щелепі. Після обговорення варіантів ортопедичної реабілітації було прийнято рішення про видалення зуба 33 та встановлення шести дентальних імплантатів з подальшим протезуванням.
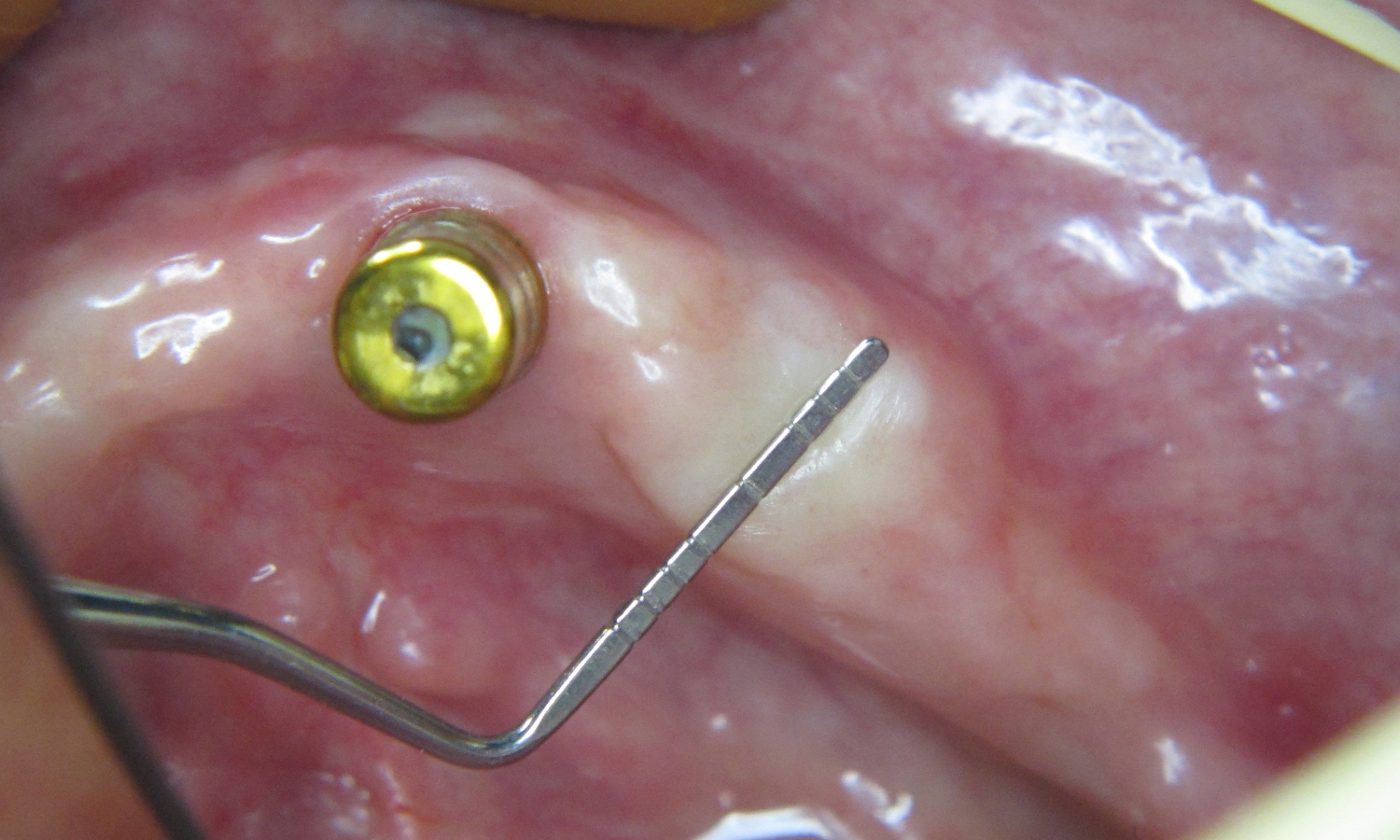
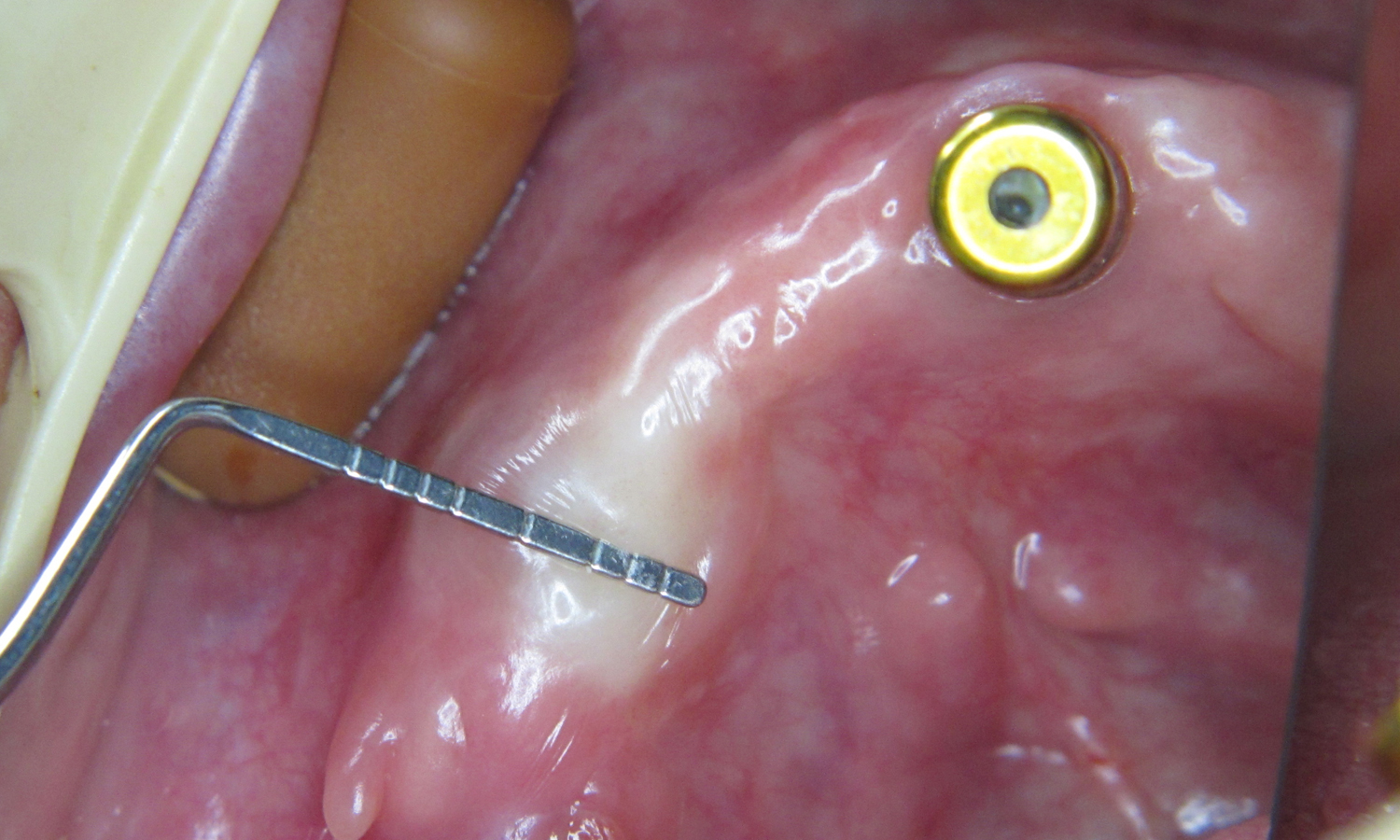
Об’єктивно: зуб 33 має рухливість III ступеня, альвеолярний паросток має ширину 5.2 мм та пірамідальну форму. Висота альвеолярного гребеня в дистальній ділянці 7 мм. Тонкий біотип пародонту (мал. 1, 2).
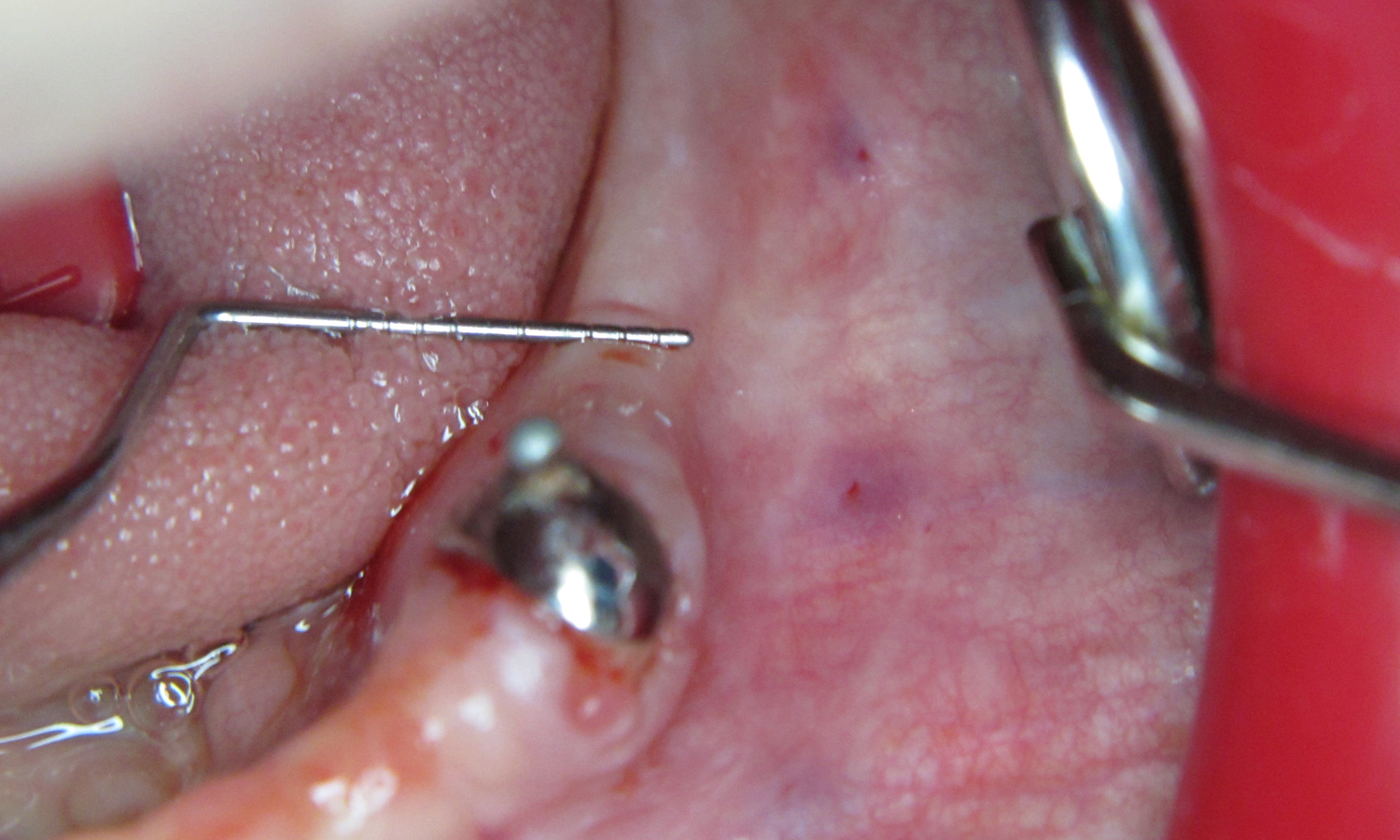
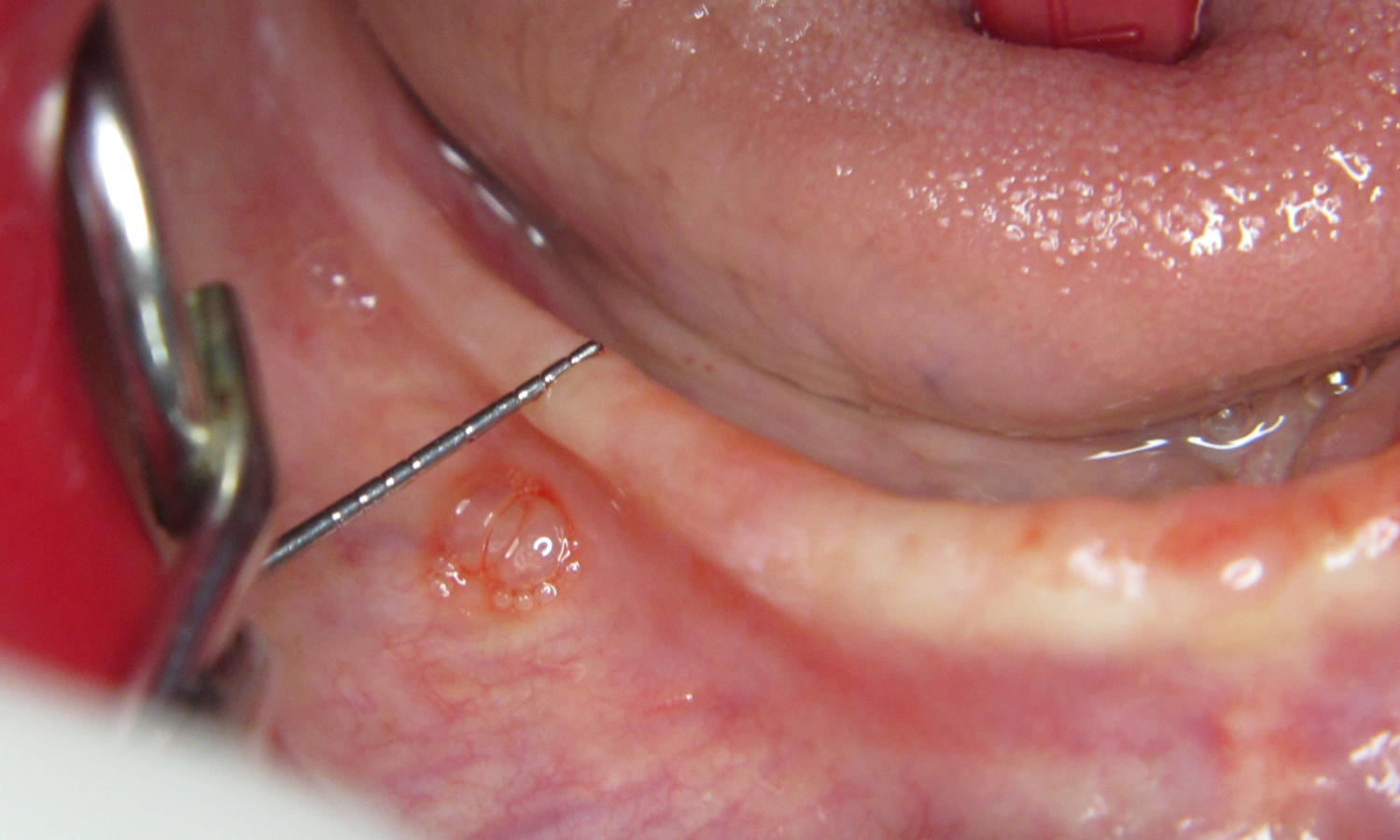
Прийнято рішення про проведення дентальної імплантації в комбінації з кістковою аугментацією за методикою розщеплення альвеолярного гребеня в поєднанні з м’якотканинною аугментацією шляхом пересадки сполучнотканинного трансплантата.
Оскільки ширина кістки 5.2 мм, ми розуміємо, що після розведення кортикальних пластинок їх товщина буде не меншою ніж 2 мм. При такій товщині кортикальної кістки, звісно за умов атравматично проведеної операції, ризик дигесценцій навколо імплантату не великий, але є ризик резорбції по верхівці альвеолярного гребеня (ремоделювання кістки) за рахунок тонкої слизової та неможливості забезпечення біологічної ширини. Саме тому ми вирішили формувати неповний клапоть з метою збереження окістя та подальшу пересадку сполучнотканинного трансплантата.
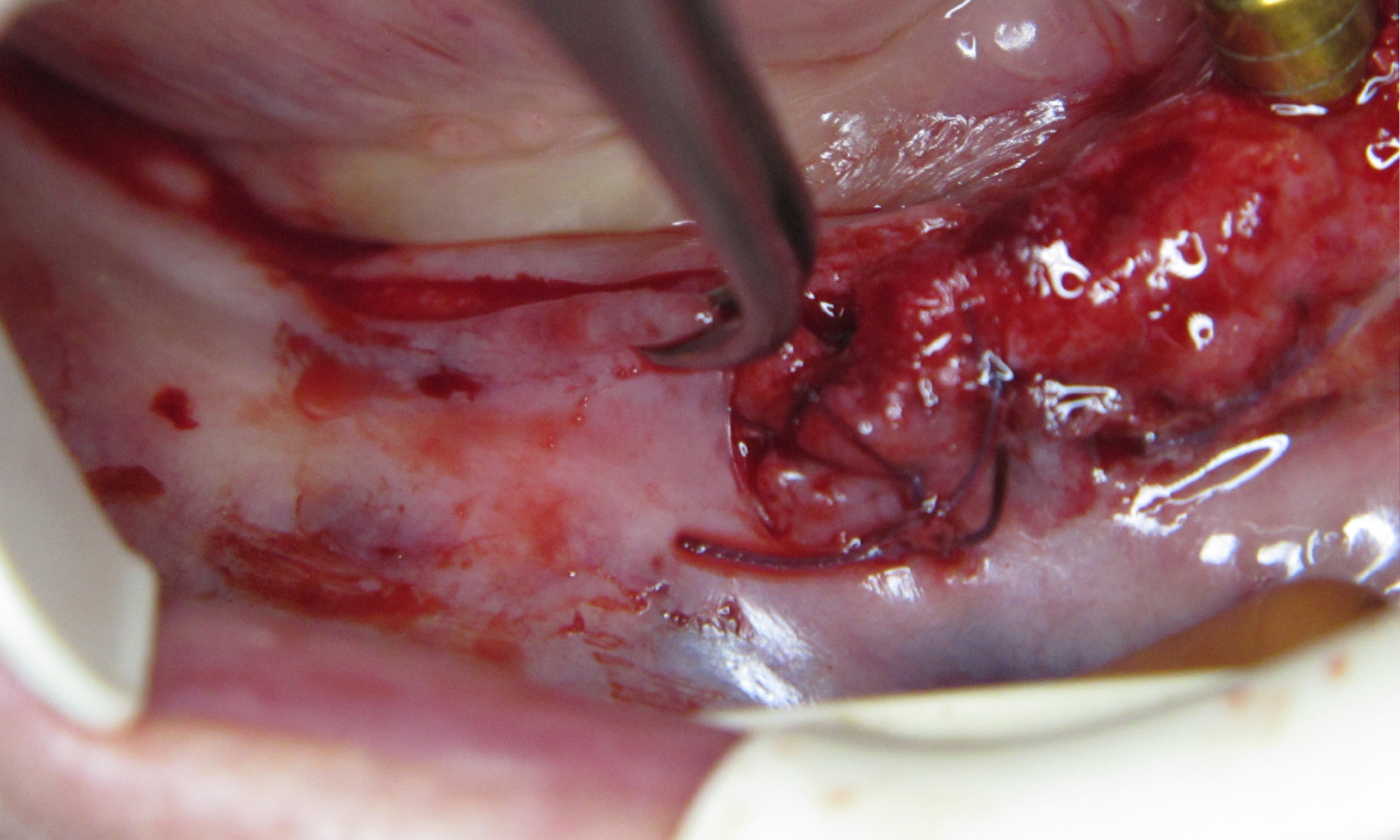
Під інфільтраційною анестезією (Ubistesin 4%) видалено зуб 33 та проведено розтин слизової, підслизової основи та окістя. Гострим шляхом відсепаровано колагенові та еластичні волокна від окістя та поверхневого клаптя (мал. 3).
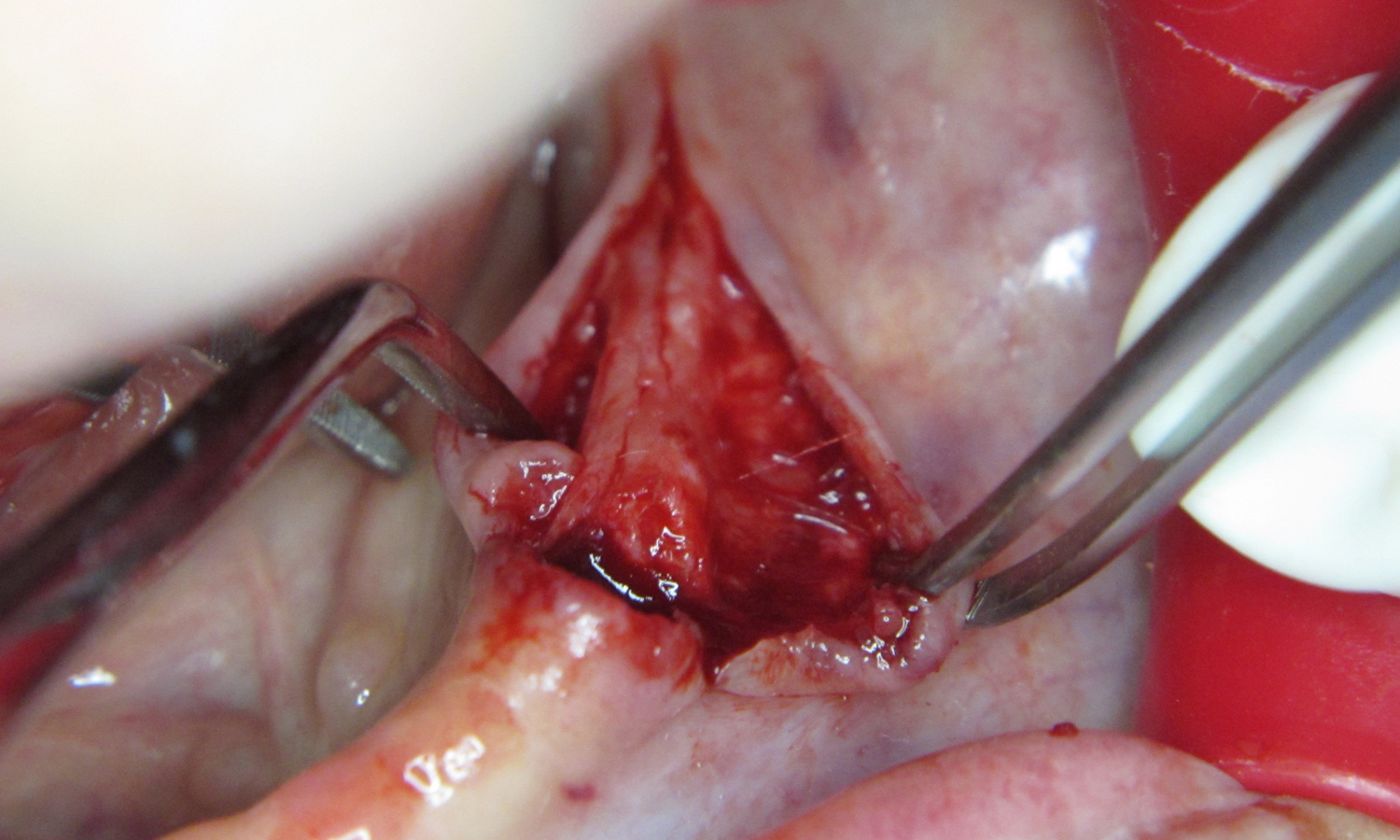
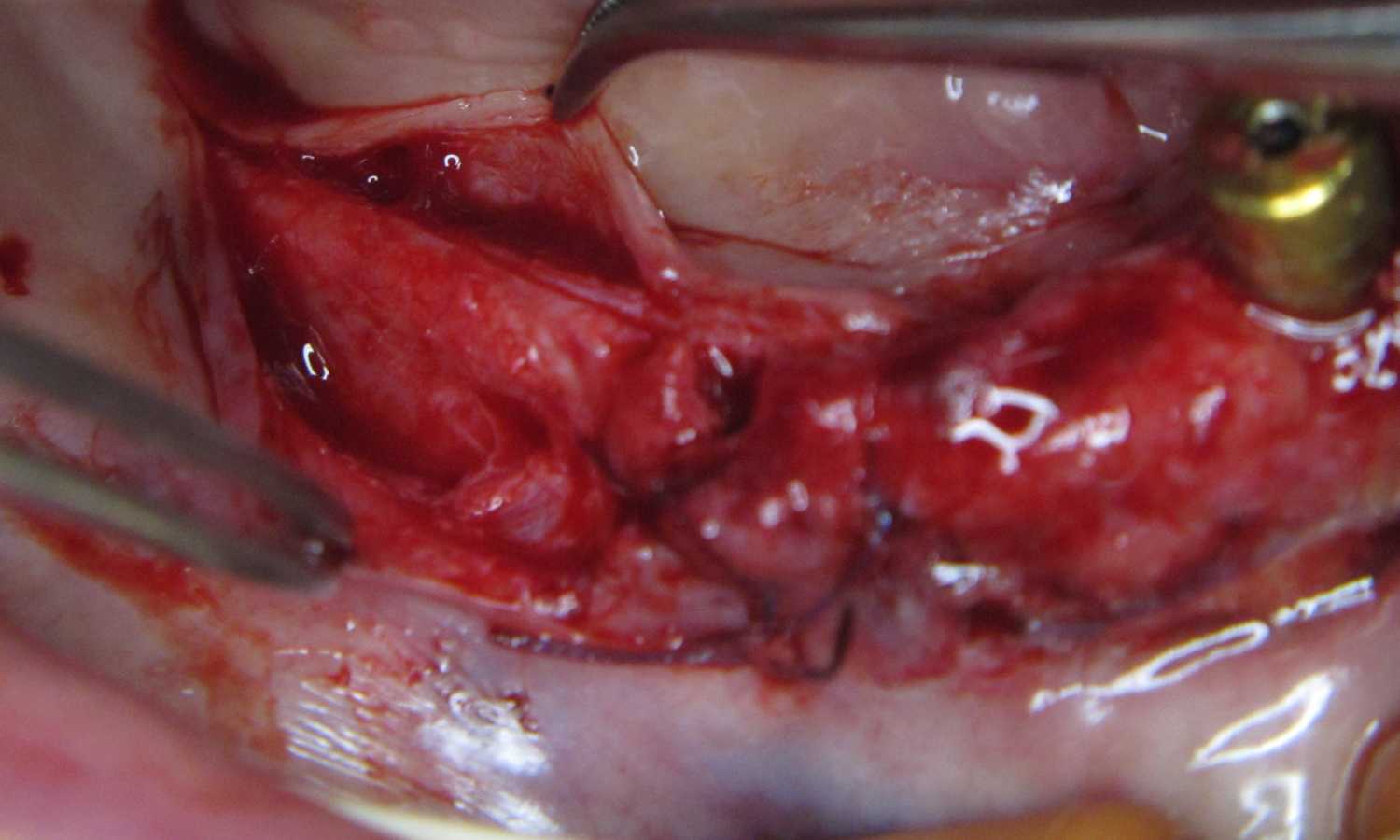
Через ділянку розтину окістя проведено розпил кортикальної пластинки. Далі, використовуючи за протоколом насадки для розщеплення апарату Piezotome Solo (Satelec, Akteon), розведено краї альвеолярного гребеня та сформовано ложе для імплантатів (мал. 4).
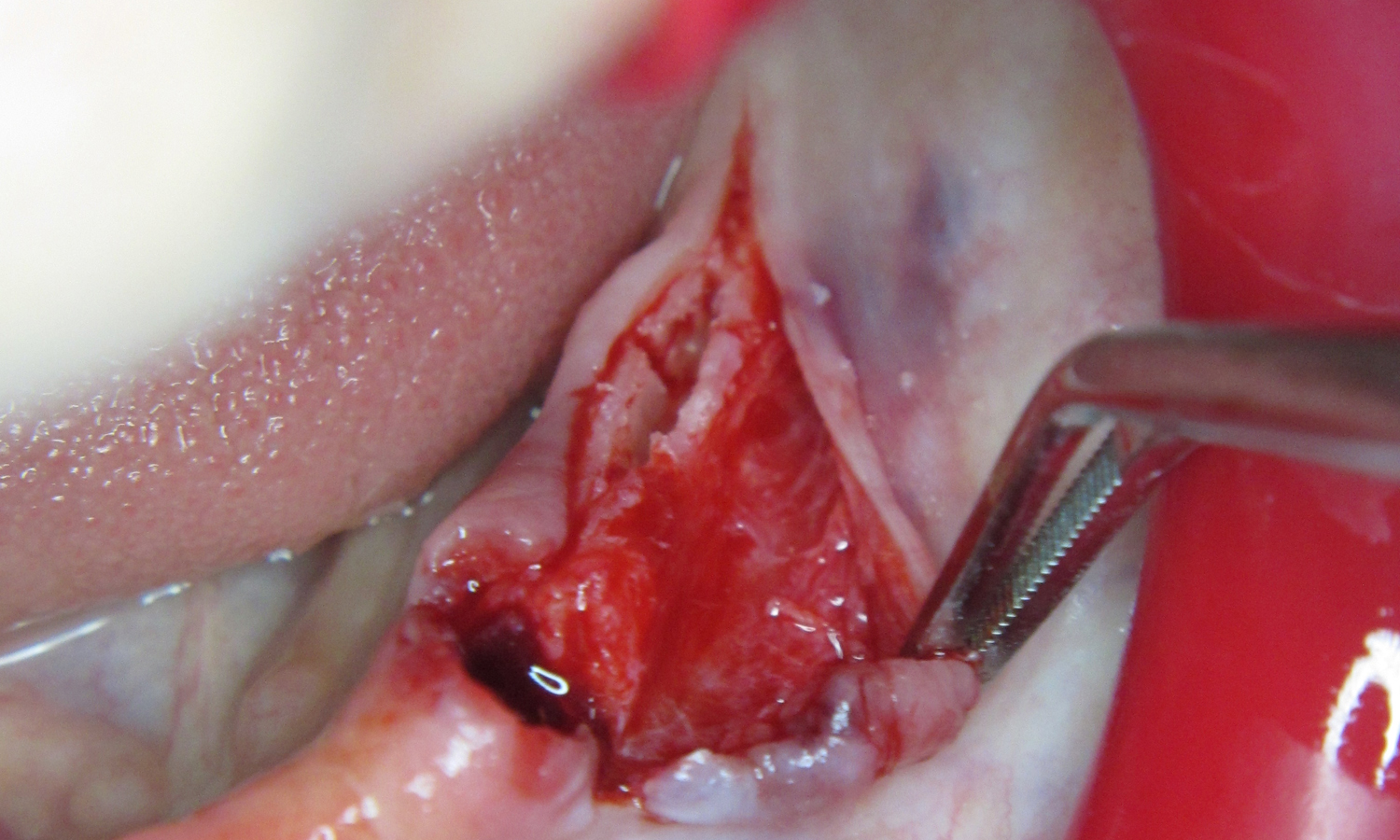
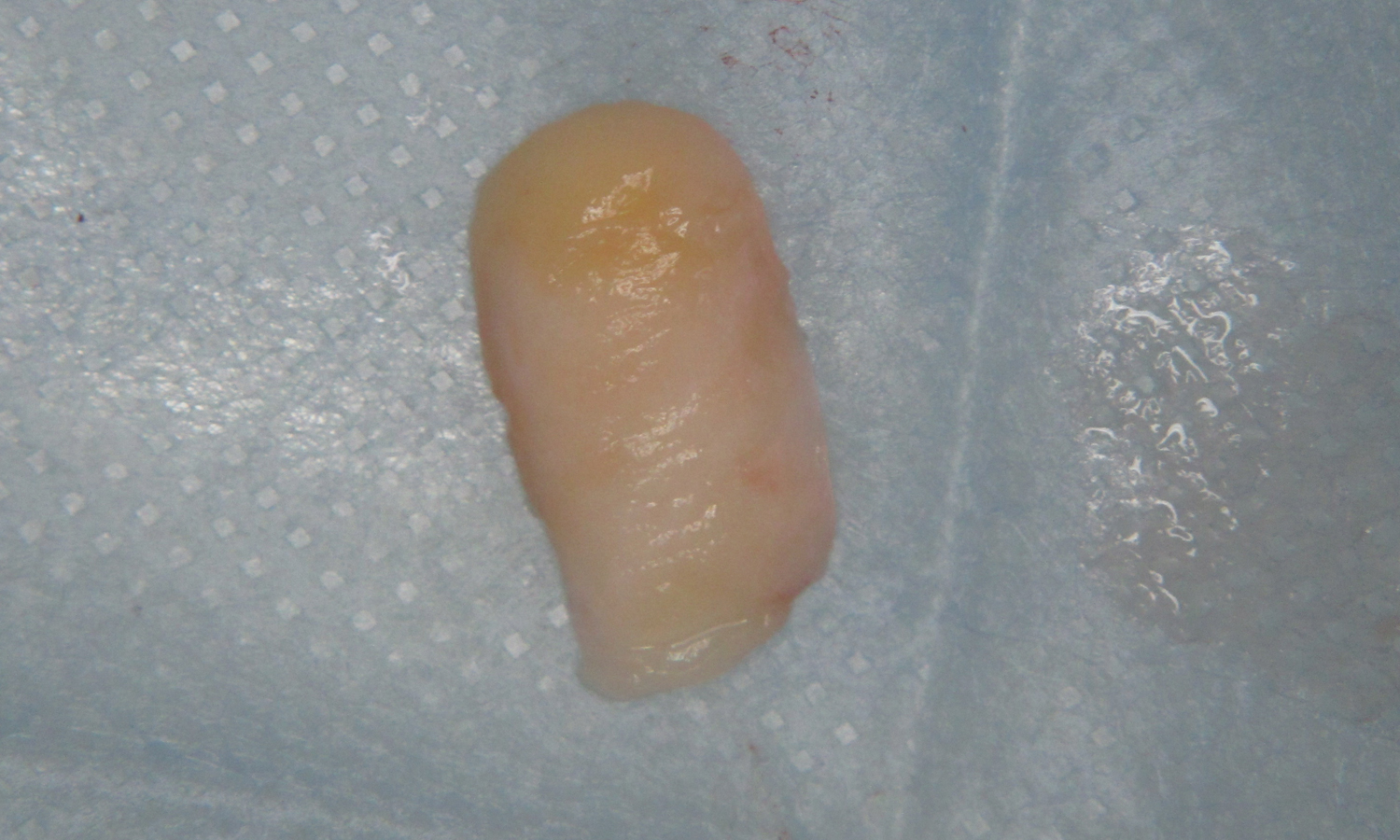
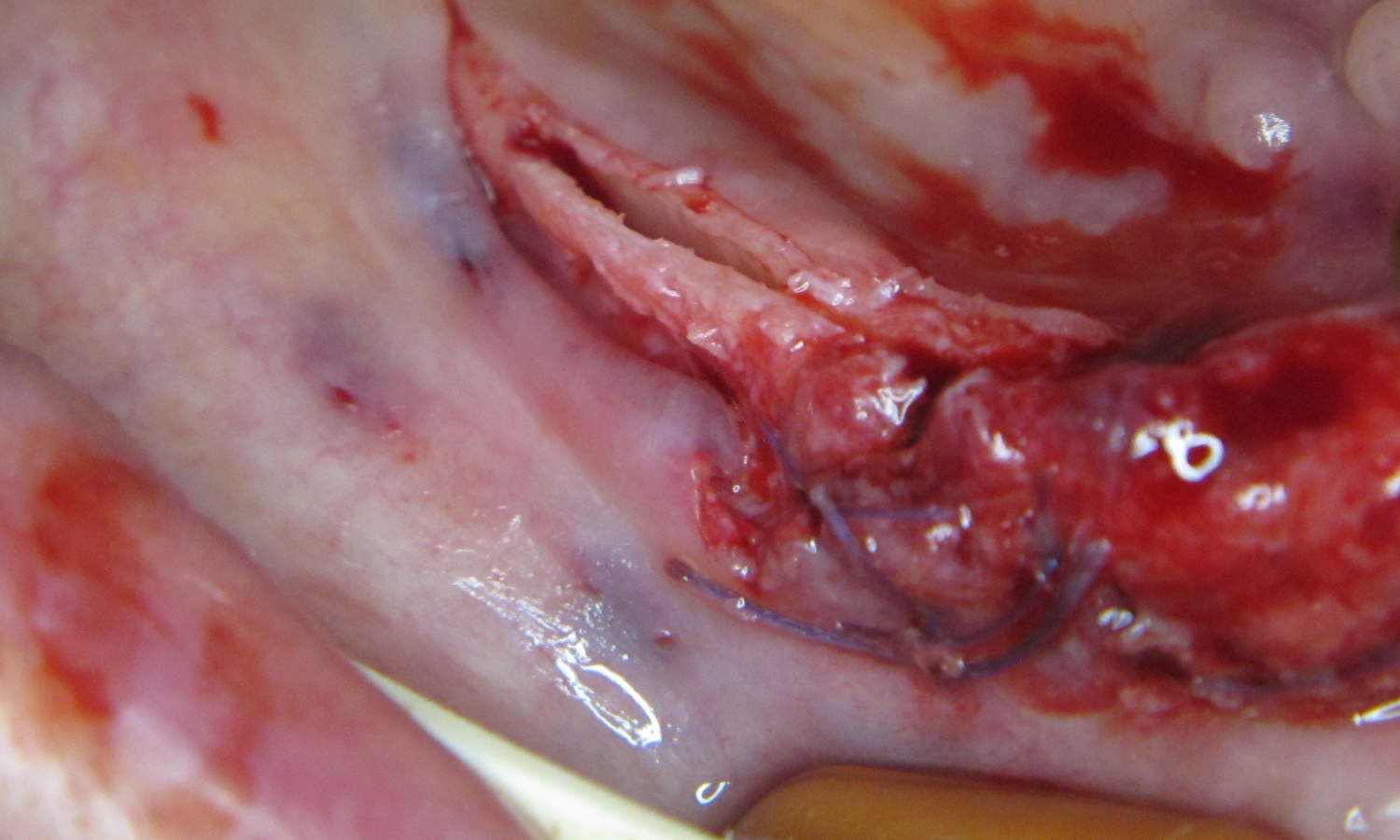
Встановлено дентальні імплантати. Аугментація (заповнення щілини між двома кортикальними пластинками) проведена матеріалом BIO GEN mix (Biotek). З піднебіння виділено ясеневий трансплантат середньої товщини (1.5 мм), деепітелізовано (мал 5) та фіксовано до окістя шовним матеріалом, що резорбується (PGA 3.0 та 5.0) (мал. 6).
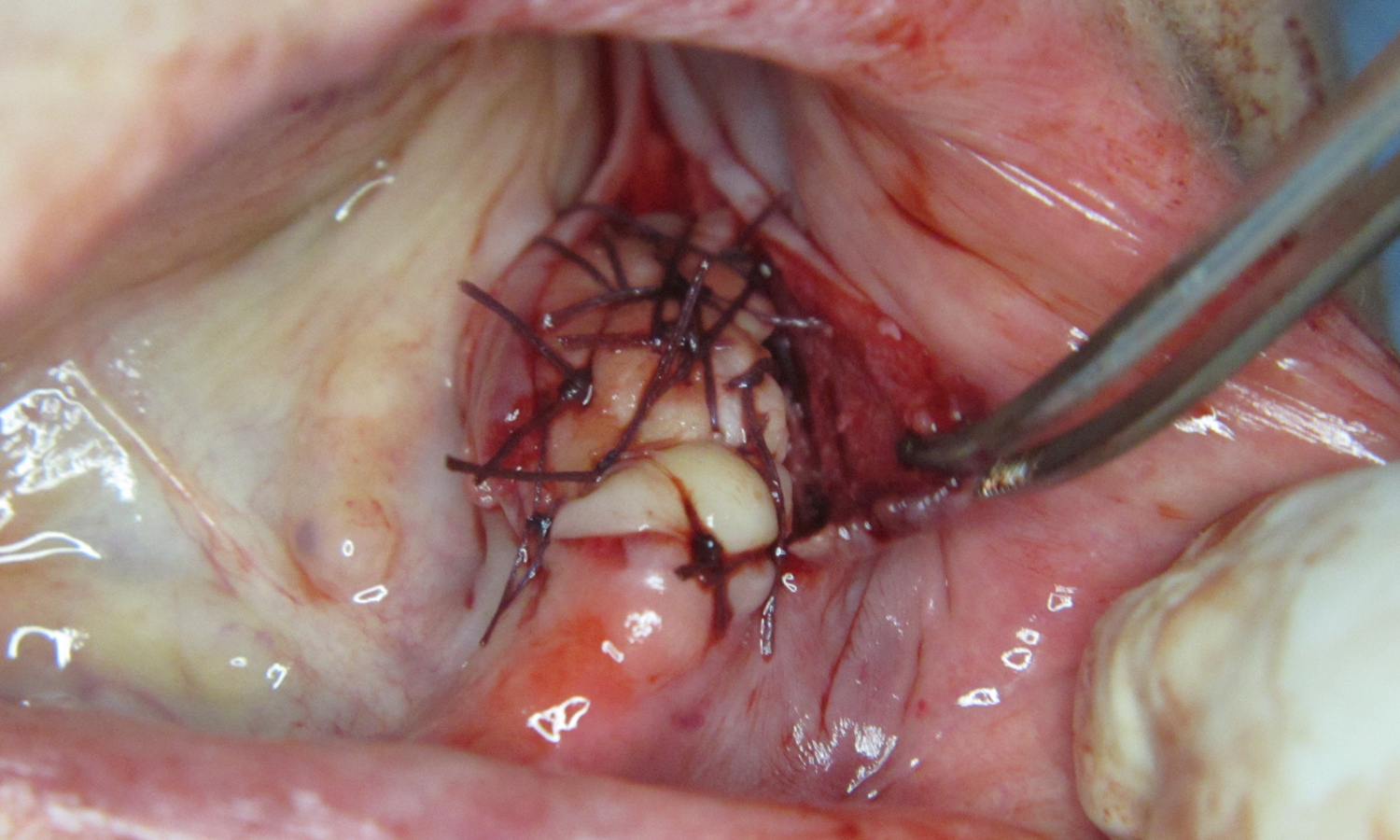
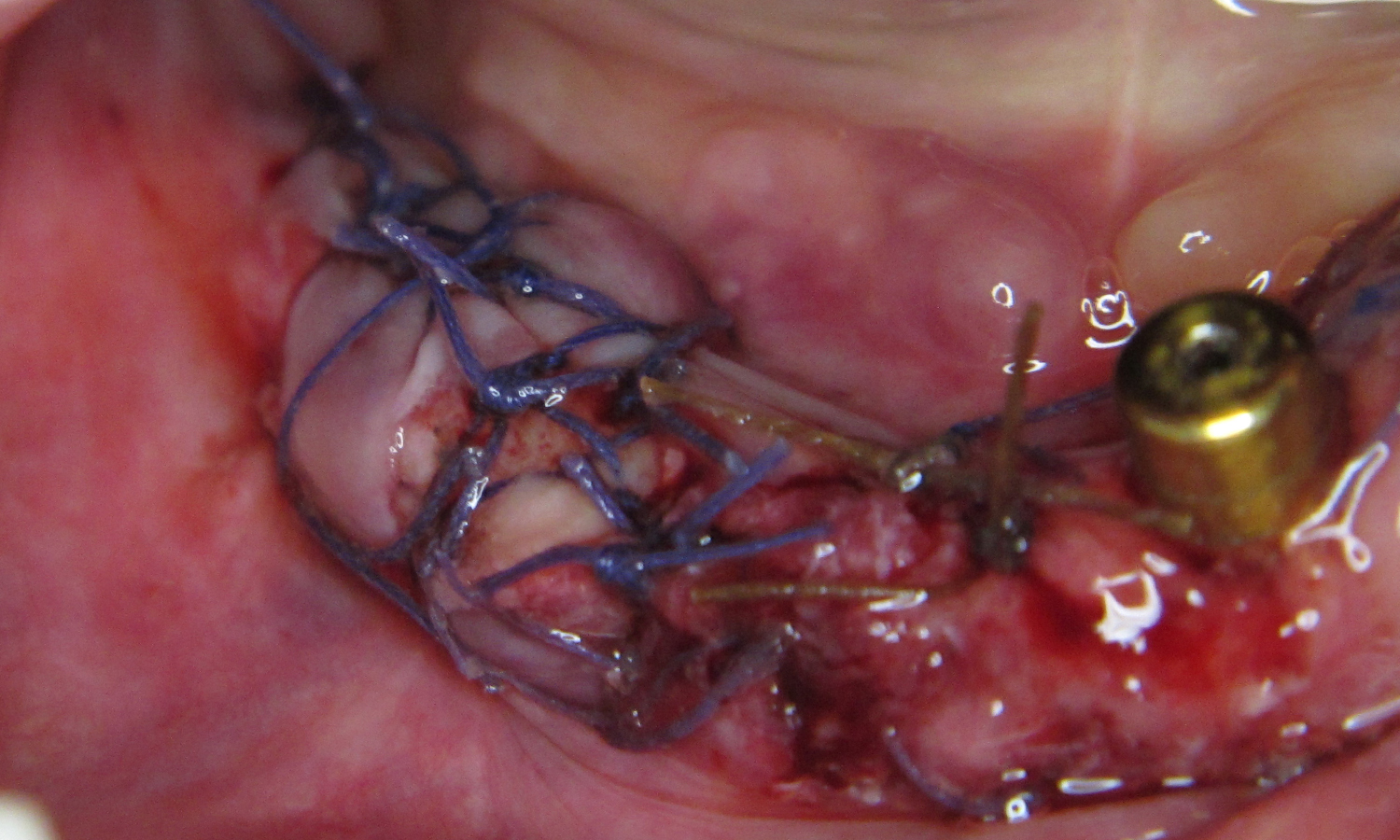
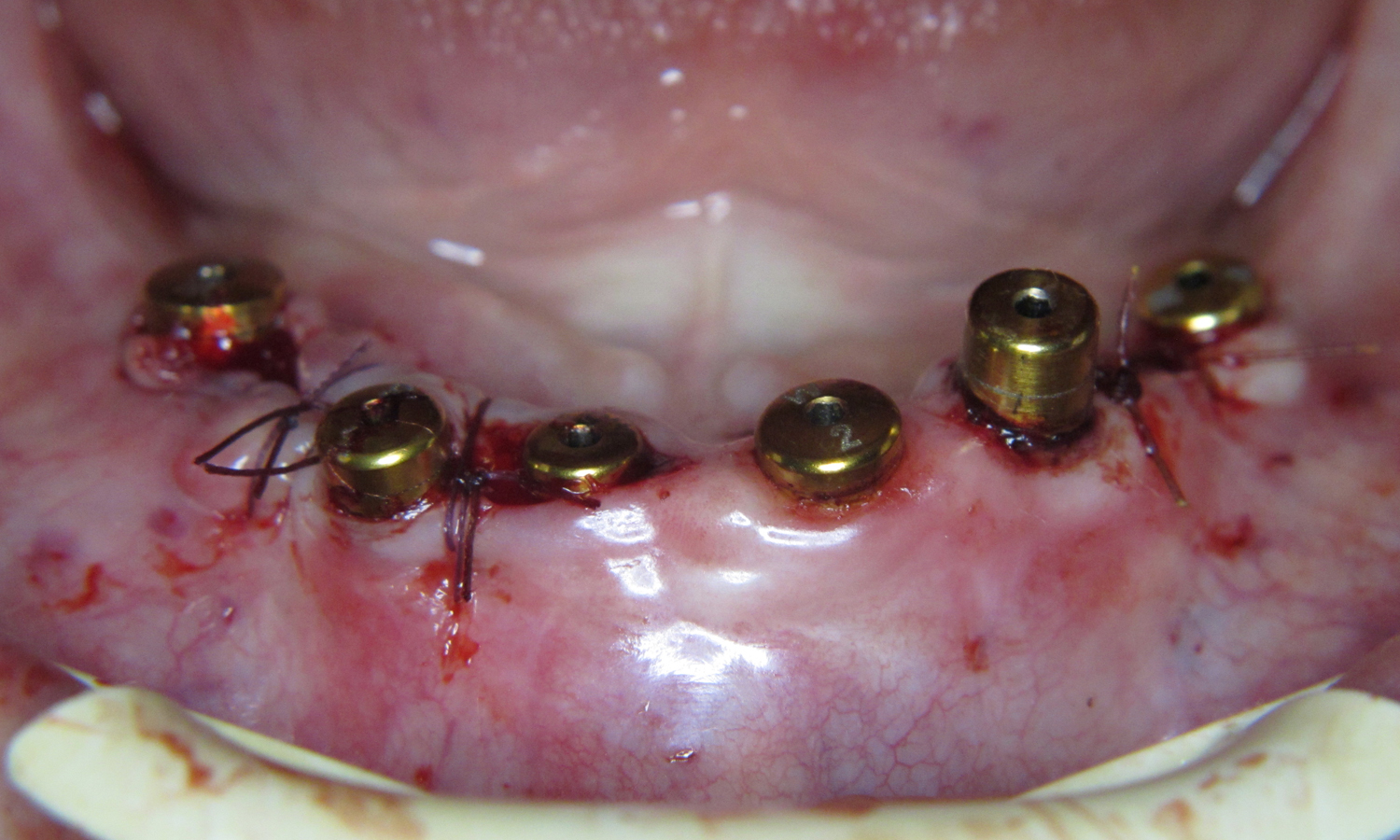
При фіксації було збережено всі загальні принципи роботи з вільними трансплантатами. Розщеплений клапоть розміщено поверх, фіксовано перехресними та вузловими швами. Також обов’язковим було накладання окісних швів для профілактики гематоми та забезпечення живлення поверхневого клаптя. Аналогічна процедура проведена з протилежної сторони та у фронтальній ділянці з єдиним вийнятком, що у ділянці різців не проводили пересадку трансплантата, а присінок сформували за методикою апікальнозміщеного клаптя та переміщення еластичних та колагенових волокон. Імплантати занурено нижче рівня кістки, окістя над імплантатами ушито PGA 6.0 Serafit (Weissner) (мал. 7 – 12).
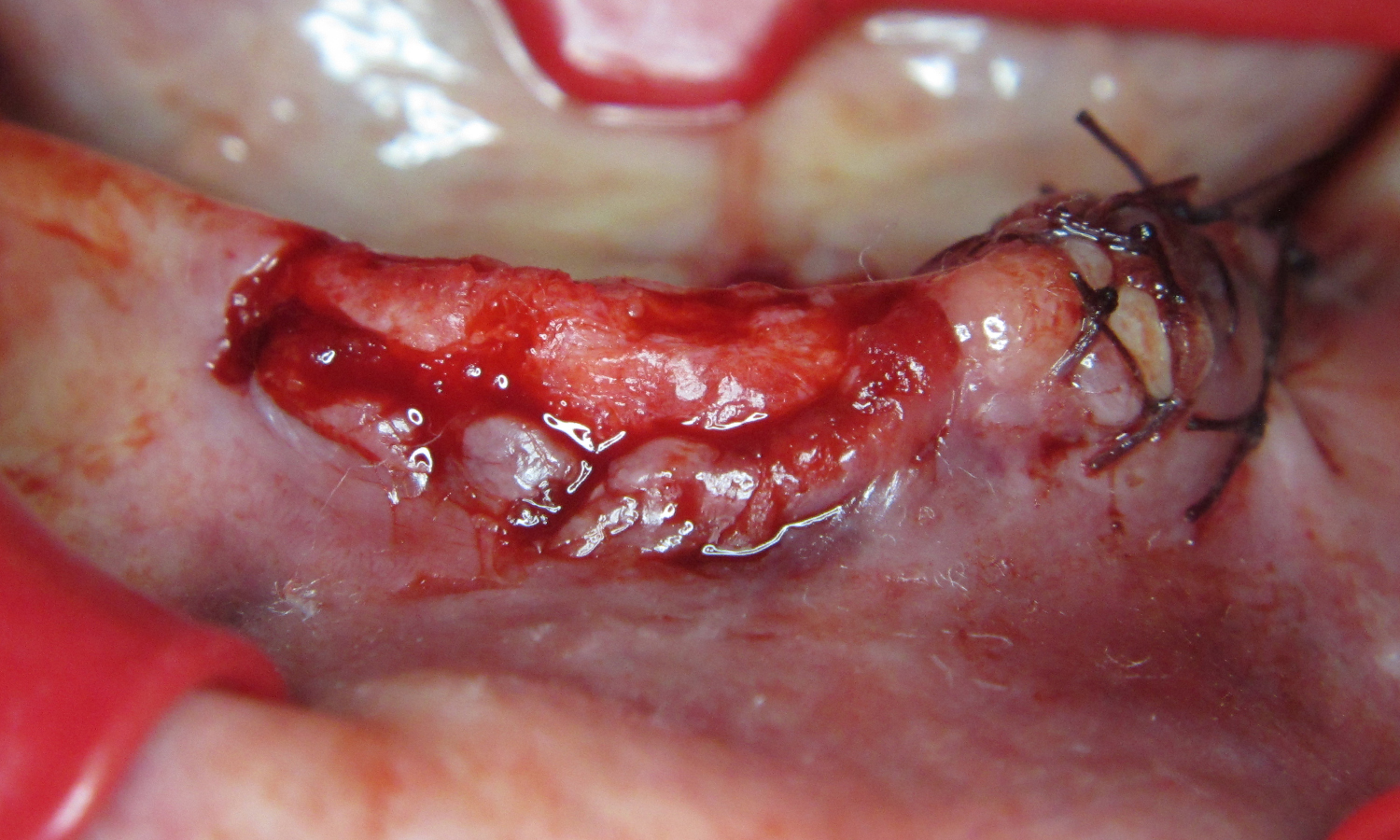
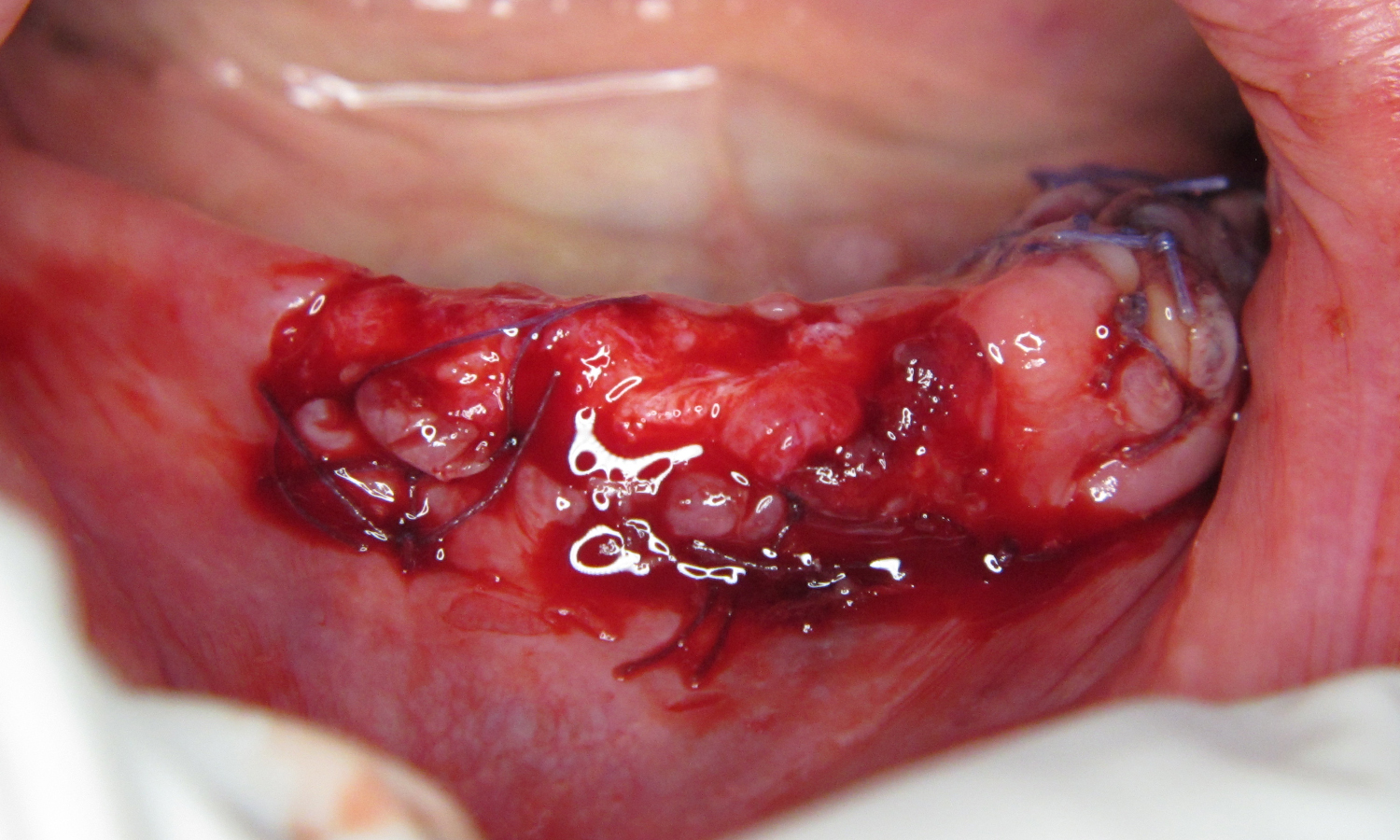
 За допомогою такої оперативної тактики вдається досягти збільшення ширини альвеолярного паростка, товщини м’яких тканин та збільшення зони прикріплених кератинізованих ясен, що на другому етапі значно полегшують маніпуляції та дозволяють запобігти резорбції альвеолярної кістки в подальшому (мал. 13 – 15).
За допомогою такої оперативної тактики вдається досягти збільшення ширини альвеолярного паростка, товщини м’яких тканин та збільшення зони прикріплених кератинізованих ясен, що на другому етапі значно полегшують маніпуляції та дозволяють запобігти резорбції альвеолярної кістки в подальшому (мал. 13 – 15).
Матеріали та методи.
У дослідження було включено 26 пацієнтів. Критеріями відбору пацієнтів для включення в дослідження були: ширина альвеолярного гребеня від 2,9 до 5.5 мм, можливість встановлення імплантатів у вірну протетичну позицію, відсутність шкідливих звичок, тощо. З дослідження не були виключені пацієнти з цукровим діабетом у стадії компенсації та пацієнти, які приймають замісну терапію за умов погодження з лікарем, який є куратором пацієнта. Розпил кортикальної кістки виконували за допомогою оборотної фрези для кутового наконечника, турбінного хірургічного бора або за допомогою апарата Piezotome Solo (Satelec, Aсteon). Створений кістковий дефект заповнювали кістковим матеріалом BIO GEN mix (Bioteсk). Імплантати встановлювали на 1.5 - 2 мм нижче рівня кістки. Бар’єрну мембрану використовували у випадку формування неповно-повно-повного клаптя, бар’єрна мембрана Hard (Bioteсk). Мембрану фіксували титановими пінами до кістки. При використанні вільного трансплантата, його фіксували швами матеріалом, що резорбується 3.0 та 5.0. Поверхневий клапоть фіксували швами з поліпропілену 4.0 та 5.0.
Результати та висновки
Дослідження проводили в період з 2008 по 2014 роки. Середній термін спостереження - 52 місяці після оперативного втручання. В дослідженні приймали участь 26 осіб. В усіх випадках, під час проведення аугментації кістки за методикою розщеплення альвеолярного гребеня, нами було встановлено дентальні імплантати від 1-го до 3-х у кожній з ділянок. Діаметр імплантатів обирався відповідно до загальних норм вибору імплантату для усунення того чи іншого дефекту. Рішення про формування виключно розщепленого клаптя та комбінацію з м’якотканинною або з латеральною аугментацією за методикою накладки, приймали за описаними вище правилами та наведеними в таблиці 1.
Нами отримані наступні результати: в усіх без виключення випадках отримано збільшення ширини альвеолярного паростка по верхівці альвеолярного гребеня на 2.5 - 4.0 мм, що складало від 30% до 110%; вертикальна резорбція складала в середньому 1.05 мм (при формуванні повного клаптя та проведенні розпилу фрезами), 0.6 мм (при формуванні повного клаптя та проведенні розпилу за допомогою Piezotome Solo), 0.4 мм (при формуванні неповного клаптя, використанні вільного трансплантата та проведення розпилу Piezotome Solo). У трьох випадках було відмічено частковий некроз трансплантата, у двох – повний некроз трансплантата. Не зважаючи на це, дані пацієнти не були виключені з дослідження. При використанні вільного трансплантата шви знімали на 10 – 16 добу. До важливих результатів слід віднести і те, що не дивлячись на частковий або повний некроз трансплантата, клінічна ситуація значно не погіршилась, а через півроку та більший термін клінічна ситуація була краще, ніж на момент протезування (оцінювання стосувалось кількості кератинізованих ясен, та рентгенологічної щільності кісткової тканини). В одному з випадків ми отримали майже повний некроз поверхневого клаптя, який пов’язуємо з утворенням гематоми та поганим контролем окісного шва, але повне приживлення трансплантату. Ще в одному з випадків ми отримали некроз вільного клаптя, але клінічна картина не вимагала додаткової роботи з м’якими тканинами.
За нашими спостереженнями зменшення травми на кожному етапі, під час роботи за досить травматичною методикою розщеплення альвеолярного гребеня, може значно поліпшити кінцевий результат, що збігається з дослідженнями інших авторів. Впровадження нових методів виконання класичних маніпуляцій, таких як використання п’єзохірургічного розпилу та розведення країв альвеолярного паростка, в поєднанні зі збереженням окістя для трофіки оперованої ділянки, зменшення кількості операцій (за можливості комбінації м’якотканинної та кісткової аугментацій) відіграє важливу роль у подальшій реабілітації пацієнтів.
Обговорення
Звісно розроблений нами підхід до комбінації методик потребує подальших спостережень з більш чисельними групами. В цьому дослідженні ми не брали до уваги особливості використання методики на нижній та верхній щелепах. Всі операції виконувала одна і та ж оперативна бригада. Обчислення результатів проводив сторонній лікар за томографічними даними які, звісно, можуть бути інтерпретовані дещо по-різному. Але результати дослідження збігаються з результатами багатьох інших досліджень на цю тему.
Також, ми вважаємо, що є досить цікавим дослідити комбінацію застосування методики розщеплення альвеолярного паростка та ортодонтичного переміщення зубів у ділянку розщеплення задля зменшення строків ортодонтичного лікування.
Ми вважаємо, що методика розщеплення альвеолярного паростка хоч і є достатньо старою, але не втрачає свою актуальність. Більш того, із застосуванням нових знань, тактик та апаратури - ця методика стала більш простою у виконанні та більш прогнозованою.
Програма нового курсу Віктора Дегасюка "Комбіновані методики аугментації"
Література
1. Osborn J.F. Die alveolarextensionsplastik. Quintessenz 1985; 39: 1: 9—14.
2. Scipioni A., Bruschi G.B., Calesini G. The edentulous ridge expansion technique: a five-year study. Int Periodontics Restorative Dent 1994; 14: 5: 451—459.
3. Simion M, Baldoni M, Zaffe D. Jawbone enlarge-ment using immediate implant placement associated with a splitcrest technique and guided tissue regeneration. Int Periodontics Restorative Dent 1992;12: 462 – 473.
4. Vercelloti T. Piezoelecctric surgery in implantology: a case report — a new piezoelectric ridge expansion technique. Int J Periodontics Resto Dent 2000; 4: 359—369
5. Giles B. Chorroks. The Controlled Assisted Ridge Expansion Technique for Implant Placement in the Anterior Maxilla: A Technical Note. Int J Periodontics Restorative Dentistry 2010; 30: 495 – 501
6. Summers RB. The osteotome technique: Part 2 – The ridge expansion osteomy (REO) producer. Compendiuv 1994; 15: 424 – 426.
7. Ueli Grunder, Hans-Peter Spielmann, Daniel Snetivy. Developent, in Vitro Testing, and Clinic Use of a 3.5 mm-diameter Zirconia Abutment. Eur J Esthet Dent 2010:5; 158-170,{The international journal of PERIODONTICS & RESTORATIVE DENTISTRY №1(1)2011 }
8. Renzo Bassetti et all. Piezoelectric Alveolar Ridge-Splitting Technique with Simultaneous Implant Placement: A Cohort Study with 2-Year Radiographic Results.Int J Oral Maxillofac Implants 2013;28(6):1570-158
9. Параскевич В.Л. Дентальная имплантология, Минск, 2006
10. Февралёва А. Ю., Давидян А. Л. Атлас пластической хирургии мягких тканей вокруг имплантатов. «Поли медиа пресс», Москва 2008 г.
11. Penarrocha-Diago M. Rambla-Ferrer J.,Perez V., Perez-Garrirues H. Benign paroxysmal vertigo secondary to placement of maxillary implants using the alveolar expansion technique with osteotomes: A study of 4 cases. Int J Oral Maxillofac Implans 2008;23:129-132
Програма нового курсу Віктора Дегасюка "Комбіновані методики аугментації"
-
Лікування захворювань СНЩС за допомогою...
23.10.2019
Статті -
Вплив корекції оклюзії за допомогою...
17.04.2019
Статті
-

20 років на ринку
стоматології -

Вся продукція
сертифікована -

Обслуговування
в сервісному центрі -

Поставки безпосередньо від
виробників
Авторизуватись
Войти
Регистрация
Восстановить пароль
Данные для входа будут высланы вам на Email
Заявка на сервисное обслуживание
Для идентификации оборудования укажите еще несколько моментов.
Замовити дзвінок
Заповніть ще кілька полів
Инструкци прийдет вам на почту
Заполните данные поля
Залишити заявку
Заповніть дані поля
